Veel mensen komen de term ioniseren van water tegen wanneer ze zich verdiepen in drinkwater.
Maar wat betekent dat eigenlijk?
Ionisatie klinkt technisch, maar het principe erachter is vrij eenvoudig. In deze blog leg ik uit wat ionisatie is en wat er met water gebeurt tijdens dat proces.
Het verschil tussen filteren en ioniseren
Allereerst wil ik voor de duidelijkheid het volgende benoemen: filteren en ioniseren worden vaak in één adem genoemd, maar het zijn twee verschillende processen.
Filteren
- verwijdert ongewenste stoffen uit water
- werkt met bijvoorbeeld koolstoffilters of membranen
Ioniseren
- verandert de elektrische lading van opgeloste mineralen
- gebeurt via elektrolyse
- in een ionisatieapparaat zit vaak ook een filter, dus het ioniseren is extra
In tegenstelling tot filteren verandert ionisatie niet zozeer welke stoffen uit het water worden verwijderd, maar wat er tijdens het elektrochemische proces met de opgeloste stoffen gebeurt. Wat ionisatie daardoor extra oplevert beschrijf ik uitgebreid in de blog: filtreren of ioniseren.
Wat betekent ioniseren?
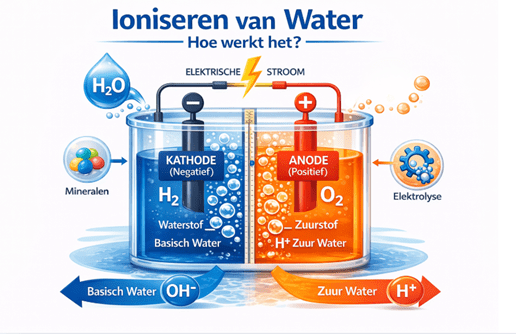
Geregeld krijg ik de vraag wat ioniseren precies is. Eigenlijk komt het er simpelweg op neer dat water onder invloed van elektriciteit wordt gesplitst. Daarbij ontstaan twee waterstromen met verschillende eigenschappen: een meer zure en een meer basische stroom. De twee waterstromen worden in het apparaat van elkaar gescheiden door een membraan, zodat het basische en zure water apart kunnen worden afgevoerd.
Het splitsen van water gebeurt doordat er een elektrische stroom door het water wordt geleid. Dit proces heet elektrolyse. Tijdens die elektrolyse ontstaan geladen deeltjes, zogenaamde ionen. Dat ontstaan van ionen noemen we ionisatie.
Bij een waterionisator wordt de stroom op ionisatieplaten gezet waar het water langs stroomt. Hierdoor vindt er elektronenverlies of opname plaats en zo ontstaan er ionen. Dit zijn positief of negatief geladen deeltjes.
Tegenwoordig zijn er ook apparaten op de markt die waterstofgas in water oplossen, zoals zogenaamde hydrogenflessen. Deze maken meestal gebruik van een kleine elektrolysecel zonder scheiding van waterstromen. Daardoor werkt het proces anders en wordt er geen afzonderlijke zure en basische waterstroom gevormd.
Wat gebeurt er met water tijdens ionisatie?
Wanneer water via elektrolyse wordt behandeld, gebeurt er in grote lijnen drie dingen:
- er wordt een elektrisch veld aangelegd via elektroden (ionisatieplaten)
- opgeloste mineralen in het water zorgen ervoor dat de elektrische stroom kan worden geleid waardoor de reacties kunnen plaatsvinden.
- het water wordt gescheiden in twee stromen met verschillende eigenschappen
Je kunt het een beetje vergelijken met twee polen die verschillende deeltjes aantrekken. Door de elektrische spanning bewegen bepaalde ionen naar de ene kant en andere ionen naar de andere kant. In die omgeving vinden vervolgens chemische reacties plaats waarbij onder andere waterstofgas en zuurstof ontstaan.
Elektrolyse wordt overigens niet alleen bij drinkwater toegepast. Het wordt ook gebruikt in bijvoorbeeld industrie, chemie en bij het maken van bepaalde metalen.
Het scheikundige proces van ionisatie
Om te begrijpen wat er gebeurt bij het ioniseren, is het goed om even naar het scheikundig proces te kijken. Vereenvoudigd kun je zeggen dat watermoleculen zich kunnen opsplitsen in H⁺ en OH⁻ ionen.
H₂O → H⁺ + OH⁻
Dat betekent: watermoleculen kunnen zich opsplitsen in deeltjes met verschillende lading
- H⁺ (waterstofion) → positief geladen
- OH⁻ (hydroxide-ion) → negatief geladen
In een ionisatiekamer bewegen die ionen naar de verschillende elektroden.
Bij de elektroden ontstaan er twee reacties:
Bij de kathode (negatieve elektrode) wordt er water gereduceerd. Dit betekent dat er elektronen, die worden geleverd door de elektrische stroom van het apparaat, worden toegevoegd. Via de stroombron worden elektronen naar de negatieve elektrode (de kathode) geleid. Daar kunnen watermoleculen deze elektronen opnemen, waardoor de reactie kan plaatsvinden.
2 H₂O + 2 e⁻ → H₂ + 2 OH⁻
Resultaat:
- er ontstaat waterstofgas (H₂)
- er blijven OH⁻ ionen in het water achter
Daarom wordt dit water basischer (alkalischer).
Bij de anode (positieve elektrode) gebeurt het tegenovergestelde:
2 H₂O → O₂ + 4 H⁺ + 4 e⁻
Resultaat:
- er ontstaat zuurstofgas (O₂)
- er blijven H⁺ ionen achter
Daarom wordt dit water zuurder.
Geïoniseerd water en waterstofgas
Zoals ik al benoemde ontstaat er tijdens de elektrolyse bij de kathode waterstofgas (H2). Dit is een gas met bijzondere eigenschappen, waar ik al eens een blog over schreef. Je vindt hem hier.
Het waterstofgas dat ontstaat:
- ontsnapt als belletjes (deze kleine gasbelletjes kunnen het water tijdelijk troebel laten lijken)
- een deel lost tijdelijk op in het water
Het basische water ontstaat dus doordat er hydroxide-ionen (OH⁻) achterblijven. In dezelfde reactie ontstaat ook waterstofgas (H₂), waarvan een deel tijdelijk in het water kan oplossen.
Nog even ter verduidelijking:
- H⁺ → zuur karakter
- OH⁻ → basisch karakter
- H₂ → opgelost gas
Over mogelijke effecten van basisch water en waterstofgas op het lichaam wordt in de wetenschappelijke literatuur onderzoek gedaan. Wie zich daar verder in wil verdiepen kan bijvoorbeeld het boek ‘De weg terug naar de jeugd’ van Sang Whang lezen. Hij gaat diep in op deze materie en beschrijft het op een begrijpelijke manier.
Door te snappen wat er tijdens ionisatie gebeurt, wordt het ook makkelijker om verschillende manieren van waterbehandeling met elkaar te vergelijken. Wil je meer basisinformatie lezen over drinkwater en verschillende manieren waarop water wordt behandeld? Dan kun je verder lezen op de waterpagina op deze website.